Menu

Czynnik V Leiden
Hubert Salamaga. Tadeusz Pietrucha. Instytut Genomiki i Medycyny Molekularnej, Centrum Medycyny Spersonalizowanej CODE sp. z o.o., Łódź.
Sprawne funkcjonowanie układu krzepnięcia krwi wymaga udziału w tym procesie wszystkich czynników krzepnięcia krwi. Układ krzepnięcia krwi zabezpiecza stałość warunków przepływu krwi zapobiegając jej wynaczynieniu (tzn. wyciekowi krwi poza uszkodzone naczynie do otaczającej go tkanki).
Jednym z czynników krzepnięcia jest czynnik V, którego wariant sekwencyjny genu, zwanego czynnikiem V Leiden charakteryzuje się tym, że zamiast argininy w pozycji 506 koduje glutaminę [1]. W warunkach fizjologicznych czynnik V, pozbawiony mutacji, jest niezbędnym kofaktorem w swojej aktywnej formie (cz. Va) wraz z cz. Xa do przekształcenia protrombiny w trombinę, co prowadzi do powstawanie skrzepu [2], ryc. 1. Białko C występujące we krwi, po aktywacji, jest „hamulcowym” procesu krzepnięcia. Działa ono poprzez utworzenie kompleksu z cz. Va i hamowanie dalszego ciągu kaskady krzepnięcia krwi [3], ryc 1. W przypadku wystąpienia mutacji V Leiden przyłączenie aktywnego białka C staje się utrudnione, a tym samym proces krzepnięcia krwi nie ulega wyhamowaniu w takim stopniu jak ma to miejsce w przypadku niezmutowanego cz. V. Następuje więc zaburzenie naturalnego procesu hamowania krzepnięcia krwi i powstanie ryzyka pojawiania się niepożądanych zakrzepów w naczyniach krwionośnych.
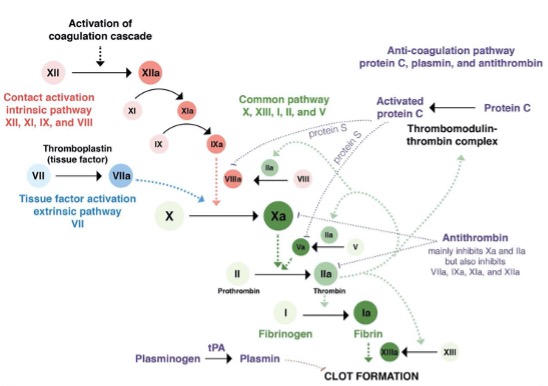
Ryc. 1. Rola czynnika V i aktywnego białka C w układzie krzepnięcia [4]
Czynnik V Leiden i protrombina 20210G>A są mutacjami, które najczęściej występują w przypadkach wrodzonej trombofili, czyli występowania skłonności do zaburzeń zakrzepowych u pacjentów obciążonych tą przypadłością.
Objawy obserwowane u nosicieli mutacji czynnika V Leiden mogą się znacznie między sobą różnić. U niektórych z nich w ciągu całego ich życia nie pojawią się powikłania zakrzepowe. Na ujawnienie się jej skutków klinicznych mogą wpłynąć dodatkowe czynniki ryzyka, np. takie jak: obecność innych mutacji wpływających na krzepliwość krwi (np. mutacji genu protrombiny 20210 G>A), ciąża, zabiegi chirurgiczne i stosowanie antykoncepcji doustnej [5,6].
Wykazano, że mutacja cz. V Leiden może mieć negatywny wpływ na przebieg i komplikacje podczas ciąży. Kobiety będące jej nosicielkami wykazują znacznie zwiększone ryzyko wystąpienia zakrzepicy podczas ciąży [7], co może być związane także z dysfunkcją naczyń łożyska.
Trombofilia matczyna, której cz. V Leiden jest istotnym czynnikiem ryzyka, może prowadzić do odklejenia się łożyska, stanu przedrzucawkowego, zahamowania wzrostu płodu, czy nawet do poronienia i utraty płodu [8].
Grupa argentyńskich badaczy (S. Udry i wsp.) wykazała, że nosicielstwo cz. V Leiden u ojców wśród par, u których dochodziło do nawracającej utraty ciąży bez znanej przyczyny, występowała 6-cio krotnie częściej niż wśród par stanowiących grupę kontrolną tego badania [9]. Tak więc predyspozycje genetyczne ojca dziecka w zakresie trombofilii, również mogą pełnić kluczową rolę w odniesieniu do utrzymania prawidłowego krążenia płodowego.
Znaczenie czynnika V w procesie krzepnięcia krwi powoduje, że mutacja Leiden jest czynnikiem ryzyka także w innych schorzeniach układu krążenia. W toku badań wykazano powiązanie obecności czynnika V Leiden z ryzykiem wystąpienia m.in. zawału serca [10]. Wyniki te wskazują na istotne statystycznie powiązanie między obecnością tej mutacji a ryzykiem wystąpienia martwicy mięśnia sercowego u osób poniżej 55 roku życia. Ponadto tak jak w przypadku innych mutacji związanych z krzepnięciem krwi mutacja ta zwiększa ryzyko wystąpienia choroby zakrzepowo-zatorowej [11].
Celem uniknięcia wyżej wymienionych komplikacji warto przed podjęciem decyzji o posiadaniu dziecka lub ważnym zabiegiem chirurgicznym, przeprowadzić badanie na nosicielstwo mutacji czynnika V Leiden. Jeśli lekarz wie, że pacjent jest nosicielem tej mutacji, może on zastosować leki zmniejszające ryzyko wystąpienia zakrzepicy.
Literatura:
- Sara A. Albagoush; Rebanta K. Chakraborty; Amy E. Schmidt. Factor V Leiden Deficiency. 2021. https://www.statpearls.com/articlelibrary/viewarticle/21577/?utm_source=pubmed&utm_campaign=CME&utm_content=21577
- Thorelli E, Kaufman RJ, Dahlbäck B. The C-terminal region of the factor V B-domain is crucial for the anticoagulant activity of factor V. J Biol Chem. 1998 Jun 26;273(26):16140-5. doi: 10.1074/jbc.273.26.16140. PMID: 9632668.
- De Stefano V, Leone G. Resistance to activated protein C due to mutated factor V as a novel cause of inherited thrombophilia. Haematologica. 1995 Jul-Aug;80(4):344-56. PMID: 7590506.
- https://step1.medbullets.com/hematology/111020/factor-v-leiden.
- Yusuf M, Gupta A, Kumar A, Afreen S. Mechanism and pathophysiology of activated protein C-related factor V Leiden in venous thrombosis. Asian J Transfus Sci. 2012 Jan;6(1):47-8. doi: 10.4103/0973-6247.95053. PMID: 22623845; PMCID: PMC3353632.
- van Vlijmen EF, Wiewel-Verschueren S, Monster TB, Meijer K. Combined oral contraceptives, thrombophilia and the risk of venous thromboembolism: a systematic review and meta-analysis. J Thromb Haemost. 2016 Jul;14(7):1393-403. doi: 10.1111/jth.13349. Epub 2016 Jun 16. PMID: 27121914.
- Rodger MA, Paidas M, McLintock C, Middeldorp S, Kahn S, Martinelli I, Hague W, Rosene Montella K, Greer I. Inherited thrombophilia and pregnancy complications revisited. Obstet Gynecol. 2008 Aug;112(2 Pt 1):320-4. doi: 10.1097/AOG.0b013e31817e8acc. Erratum in: Obstet Gynecol. 2008 Dec;112(6):1392. Claire, McLintock [corrected to McLintock, Claire]. PMID: 18669729.
- Kinzler WL, Prasad V, Ananth CV. The effect of maternal thrombophilia on placental abruption: histologic correlates. J Matern Fetal Neonatal Med 2009; 22: 243–8.
- S. Udry, F. M. Aranda, J. O. Latino and G. F. de Larranaga. Paternal factor V Leiden and recurrent pregnancy loss: a new concept behind fetal genetics? Journal of Thrombosis and Haemostasis, 12: 666–669.
- Doix S, Mahrousseh M, Jolak M, Laurent Y, Lorenzini JL, Binquet C, Zeller M, Cottin Y, Wolf JE. Facteur V Leiden et infarctus du myocarde: à propos d’un cas, revue systématique de la littérature et méta-analyse [Factor V Leiden and myocardial infarction: a case, review of the literature with a meta-analysis]. Ann Cardiol Angeiol (Paris). 2003 Jun;52(3):143-9. French. doi: 10.1016/s0003-3928(02)00192-0. PMID: 12938565.
- Price DT, Ridker PM. Factor V Leiden mutation and the risks for thromboembolic disease: a clinical perspective. Ann Intern Med. 1997 Nov 15;127(10):895-903. doi: 10.7326/0003-4819-127-10-199711150-00007. PMID: 9382368.
MASZ WĄTPLIWOŚCI/PYTANIA, ZADAJ JE PONIŻEJ, A MY PO KONSULTACJI ZE SPECJALISTAMI ODPOWIEMY NA TWOJE PYTANIE!
Menu

Czynnik V Leiden
Hubert Salamaga. Tadeusz Pietrucha. Instytut Genomiki i Medycyny Molekularnej, Centrum Medycyny Spersonalizowanej CODE sp. z o.o., Łódź.
Sprawne funkcjonowanie układu krzepnięcia krwi wymaga udziału w tym procesie wszystkich czynników krzepnięcia krwi. Układ krzepnięcia krwi zabezpiecza stałość warunków przepływu krwi zapobiegając jej wynaczynieniu (tzn. wyciekowi krwi poza uszkodzone naczynie do otaczającej go tkanki).
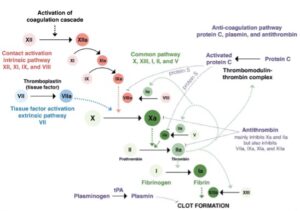
Jednym z czynników krzepnięcia jest czynnik V, którego wariant sekwencyjny genu, zwanego czynnikiem V Leiden charakteryzuje się tym, że zamiast argininy w pozycji 506 koduje glutaminę [1]. W warunkach fizjologicznych czynnik V, pozbawiony mutacji, jest niezbędnym kofaktorem w swojej aktywnej formie (cz. Va) wraz z cz. Xa do przekształcenia protrombiny w trombinę, co prowadzi do powstawanie skrzepu [2], ryc. 1. Białko C występujące we krwi, po aktywacji, jest „hamulcowym” procesu krzepnięcia. Działa ono poprzez utworzenie kompleksu z cz. Va i hamowanie dalszego ciągu kaskady krzepnięcia krwi [3], ryc 1. W przypadku wystąpienia mutacji V Leiden przyłączenie aktywnego białka C staje się utrudnione, a tym samym proces krzepnięcia krwi nie ulega wyhamowaniu w takim stopniu jak ma to miejsce w przypadku niezmutowanego cz. V. Następuje więc zaburzenie naturalnego procesu hamowania krzepnięcia krwi i powstanie ryzyka pojawiania się niepożądanych zakrzepów w naczyniach krwionośnych.

Ryc. 1. Rola czynnika V i aktywnego białka C w układzie krzepnięcia [4]
Czynnik V Leiden i protrombina 20210G>A są mutacjami, które najczęściej występują w przypadkach wrodzonej trombofili, czyli występowania skłonności do zaburzeń zakrzepowych u pacjentów obciążonych tą przypadłością.
Objawy obserwowane u nosicieli mutacji czynnika V Leiden mogą się znacznie między sobą różnić. U niektórych z nich w ciągu całego ich życia nie pojawią się powikłania zakrzepowe. Na ujawnienie się jej skutków klinicznych mogą wpłynąć dodatkowe czynniki ryzyka, np. takie jak: obecność innych mutacji wpływających na krzepliwość krwi (np. mutacji genu protrombiny 20210 G>A), ciąża, zabiegi chirurgiczne i stosowanie antykoncepcji doustnej [5,6].
Wykazano, że mutacja cz. V Leiden może mieć negatywny wpływ na przebieg i komplikacje podczas ciąży. Kobiety będące jej nosicielkami wykazują znacznie zwiększone ryzyko wystąpienia zakrzepicy podczas ciąży [7], co może być związane także z dysfunkcją naczyń łożyska.
Trombofilia matczyna, której cz. V Leiden jest istotnym czynnikiem ryzyka, może prowadzić do odklejenia się łożyska, stanu przedrzucawkowego, zahamowania wzrostu płodu, czy nawet do poronienia i utraty płodu [8].
Grupa argentyńskich badaczy (S. Udry i wsp.) wykazała, że nosicielstwo cz. V Leiden u ojców wśród par, u których dochodziło do nawracającej utraty ciąży bez znanej przyczyny, występowała 6-cio krotnie częściej niż wśród par stanowiących grupę kontrolną tego badania [9]. Tak więc predyspozycje genetyczne ojca dziecka w zakresie trombofilii, również mogą pełnić kluczową rolę w odniesieniu do utrzymania prawidłowego krążenia płodowego.
Znaczenie czynnika V w procesie krzepnięcia krwi powoduje, że mutacja Leiden jest czynnikiem ryzyka także w innych schorzeniach układu krążenia. W toku badań wykazano powiązanie obecności czynnika V Leiden z ryzykiem wystąpienia m.in. zawału serca [10]. Wyniki te wskazują na istotne statystycznie powiązanie między obecnością tej mutacji a ryzykiem wystąpienia martwicy mięśnia sercowego u osób poniżej 55 roku życia. Ponadto tak jak w przypadku innych mutacji związanych z krzepnięciem krwi mutacja ta zwiększa ryzyko wystąpienia choroby zakrzepowo-zatorowej [11].
Celem uniknięcia wyżej wymienionych komplikacji warto przed podjęciem decyzji o posiadaniu dziecka lub ważnym zabiegiem chirurgicznym, przeprowadzić badanie na nosicielstwo mutacji czynnika V Leiden. Jeśli lekarz wie, że pacjent jest nosicielem tej mutacji, może on zastosować leki zmniejszające ryzyko wystąpienia zakrzepicy.v
Literatura:
- Sara A. Albagoush; Rebanta K. Chakraborty; Amy E. Schmidt. Factor V Leiden Deficiency. 2021. https://www.statpearls.com/articlelibrary/viewarticle/21577/?utm_source=pubmed&utm_campaign=CME&utm_content=21577
- Thorelli E, Kaufman RJ, Dahlbäck B. The C-terminal region of the factor V B-domain is crucial for the anticoagulant activity of factor V. J Biol Chem. 1998 Jun 26;273(26):16140-5. doi: 10.1074/jbc.273.26.16140. PMID: 9632668.
- De Stefano V, Leone G. Resistance to activated protein C due to mutated factor V as a novel cause of inherited thrombophilia. Haematologica. 1995 Jul-Aug;80(4):344-56. PMID: 7590506.
- https://step1.medbullets.com/hematology/111020/factor-v-leiden.
- Yusuf M, Gupta A, Kumar A, Afreen S. Mechanism and pathophysiology of activated protein C-related factor V Leiden in venous thrombosis. Asian J Transfus Sci. 2012 Jan;6(1):47-8. doi: 10.4103/0973-6247.95053. PMID: 22623845; PMCID: PMC3353632.
- van Vlijmen EF, Wiewel-Verschueren S, Monster TB, Meijer K. Combined oral contraceptives, thrombophilia and the risk of venous thromboembolism: a systematic review and meta-analysis. J Thromb Haemost. 2016 Jul;14(7):1393-403. doi: 10.1111/jth.13349. Epub 2016 Jun 16. PMID: 27121914.
- Rodger MA, Paidas M, McLintock C, Middeldorp S, Kahn S, Martinelli I, Hague W, Rosene Montella K, Greer I. Inherited thrombophilia and pregnancy complications revisited. Obstet Gynecol. 2008 Aug;112(2 Pt 1):320-4. doi: 10.1097/AOG.0b013e31817e8acc. Erratum in: Obstet Gynecol. 2008 Dec;112(6):1392. Claire, McLintock [corrected to McLintock, Claire]. PMID: 18669729.
- Kinzler WL, Prasad V, Ananth CV. The effect of maternal thrombophilia on placental abruption: histologic correlates. J Matern Fetal Neonatal Med 2009; 22: 243–8.
- S. Udry, F. M. Aranda, J. O. Latino and G. F. de Larranaga. Paternal factor V Leiden and recurrent pregnancy loss: a new concept behind fetal genetics? Journal of Thrombosis and Haemostasis, 12: 666–669.
- Doix S, Mahrousseh M, Jolak M, Laurent Y, Lorenzini JL, Binquet C, Zeller M, Cottin Y, Wolf JE. Facteur V Leiden et infarctus du myocarde: à propos d’un cas, revue systématique de la littérature et méta-analyse [Factor V Leiden and myocardial infarction: a case, review of the literature with a meta-analysis]. Ann Cardiol Angeiol (Paris). 2003 Jun;52(3):143-9. French. doi: 10.1016/s0003-3928(02)00192-0. PMID: 12938565.
- Price DT, Ridker PM. Factor V Leiden mutation and the risks for thromboembolic disease: a clinical perspective. Ann Intern Med. 1997 Nov 15;127(10):895-903. doi: 10.7326/0003-4819-127-10-199711150-00007. PMID: 9382368.
MASZ WĄTPLIWOŚCI/PYTANIA, ZADAJ JE PONIŻEJ, A MY PO KONSULTACJI ZE SPECJALISTAMI ODPOWIEMY NA TWOJE PYTANIE!